유한양행은 알레르기 질환 치료 신약으로 개발 중인 ‘레시게르셉트(코드명 YH35324)’의 연내 기술수출(L/O)을 목표로 하고 있다. 계획대로면 2029년 허가, 2030년 매출 300억 원이 기대된다.
레시게르셉트의 가치를 높이기 위해 유한양행은 다른 기전의 알레르기 치료제와 병용요법 임상을 추진한다. 알레르기 질환의 발병 원인이 다양하다는 점에서 기존 치료제로 충분한 효과를 보지 못하는 환자들에게 유용한 옵션으로 경쟁력을 갖춘다는 전략이다.
이는 국산 31호 신약으로 상용화에 성공한 비소세포폐암 치료제 렉라자(성분명 레이저티닙)의 성공모델과 유사하다.
유한양행은 2018년 11월 존슨앤드존슨 이노베이티브 메디슨(이하 J&J, 구 얀센)에 1조7000억 원 규모로 렉라자를 기술수출했다. J&J는 자사 표적항암제 리브리반트와 렉라자의 병용요법으로 기존 글로벌 표준치료제 대비 전체 생존기간을 12개월 이상 개선했다.
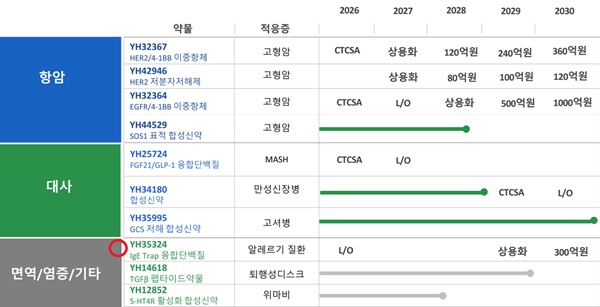
해당 알레르기 질환은 외부 물질(집먼지진드기, 꽃가루 등)에 의해 면역 반응이 일어나면 해당 물질에 대한 ‘lgE’라는 항체가 생성되면서 발병한다. 해당 물질이 다시 체내로 들어오면 생성된 lgE와 결합하면서 두드러기, 가려움, 콧물 등 증상을 유발하는 염증물질이 분비된다.
레시게르셉트는 항 lgE 계열 신약으로 혈중 수용체에 붙지 않고 떠다니는 lgE를 억제시켜 알레르기 증상을 개선한다. 경쟁약물 대비 lgE에 높은 결합력과 과민반응 등 부작용을 줄이는 방향으로 개발되고 있다.
유한양행은 지난해 10월 식품의약품안전처로부터 레시게르셉트 임상 2상을 승인 받았다. 만성 자발성 두드러기 성인 환자를 대상으로 투약 이후 12주차 두드러기 가려움 증상을 지표로 나타낸 UAS7 변화로 약효를 확인하는 시험이다. 내국인 35명을 포함해 총 150명을 대상으로 진행할 예정이다.
유럽연합(EU)과 중국에서도 임상을 진행하기 위해 임상시험신청서(IND) 제출을 준비하고 있다.
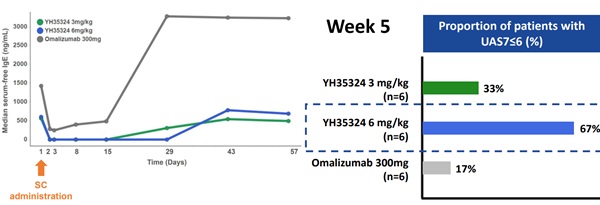
오말리주맙 투여(300mg)군은 혈중 수용체에 붙지 않고 떠다니는 lgE이 15일 이후 500ng/mL에서 29일차 3000ng/mL까지 치솟은 반면 레시게르셉트(3mg/kg) 투여군은 29일차부터 43일차 57일차 모두 500이하를 유지했다.
UAS7 지표에서도 투약 5주차 기준 증상이 잘 조절되는 수치(6이하)를 보인 시험자 비율이 오말리주맙은 17%인데 비해 레시게르셉트는 3mg/kg 투여군에서 33%, 고용량인 6mg/kg에선 67%까지 나타났다.
이외에도 기존 약물에 반응하지 않는 만성 특발성 두드러기 증상에도 치료제로 쓰일 수 있는 가능성을 보였다는 게 회사 측 설명이다.
글로벌 알레르기 치료제 시장 규모는 32조 원 수준으로 알려졌다. 만성 특발성 두드러기 외에도 음식 알레르기, 천식, 아토피 등 다양한 형태로 나타나고 있다.
유한양행 관계자는 “뉴코 설립 후 인수합병, 자체 상용화, 렉라자처럼 기술수출 이후 개발 진행 등 파이프라인 육성에서 다양한 방법을 검토하고 있다”고 말했다.
[소비자가만드는신문=정현철 기자]



